長春新產(chǎn)業(yè)光電技術(shù)有限公司(CNI)是依托中國科學(xué)院長春光機所設(shè)立的高科技企業(yè),主要從事半導(dǎo)體激光器、固體激光器、 激光測量設(shè)備、光譜儀器、教學(xué)儀器和機器視覺產(chǎn)品的研發(fā)、生產(chǎn)和銷售,并提供光學(xué)儀器、精密機械和光學(xué)鍍膜產(chǎn)品的設(shè)計和加工。
近年來,以激光器為基礎(chǔ)的激光產(chǎn)業(yè)在全球發(fā)展迅猛。據(jù)統(tǒng)計,每年和激光相關(guān)產(chǎn)品和服務(wù)的市場價值高達(dá)上萬億美元。得益于應(yīng)用領(lǐng)域的不斷拓展,中國激光產(chǎn)業(yè)也逐漸駛?cè)敫咚侔l(fā)展期。小編將為大家介紹21類激光前沿應(yīng)用,并對激光器的選擇提供一些參考性建議。
1、數(shù)字PCR(dPCR)
數(shù)字PCR是第三代PCR技術(shù),是一種核酸分子絕對定量技術(shù)。與傳統(tǒng)qPCR技術(shù)相比,數(shù)字PCR(dPCR)具有:絕對定量、無需標(biāo)準(zhǔn)品、樣品需求低,高靈敏度,高耐受性等特點。
數(shù)字PCR一般包括兩部分內(nèi)容,即PCR擴增和熒光信號分析。在PCR 擴增階段,數(shù)字PCR一般需要將樣品稀釋到單分子水平,并平均分配到幾十至幾萬個單元中進行反應(yīng),通過特定激光來激發(fā)出通道中的熒光信號。在擴增結(jié)束后對各個反應(yīng)單元的熒光信號進行統(tǒng)計學(xué)分析,最后通過直接計數(shù)或泊松分布公式計算得到樣品的原始濃度或含量。相對于qPCR技術(shù),dPCR技術(shù)具備以下優(yōu)勢:(1)靈敏度可達(dá)單個核酸分子:檢測限低至0.001%;(2)無需標(biāo)準(zhǔn)品/標(biāo)準(zhǔn)曲線,即可對靶分子起始量進行絕對定量;(3)特別適合基質(zhì)復(fù)雜樣品的檢測;(4)能夠有效區(qū)分濃度差異(變化)微小的樣品,有更好的準(zhǔn)確度、精密度和重復(fù)性。目前,數(shù)字PCR技術(shù)在病原體檢測、癌癥生物標(biāo)志物研究和拷貝數(shù)變異分析、基因表達(dá)分析、環(huán)境監(jiān)測、食品檢測等領(lǐng)域得到廣泛應(yīng)用。
常見的數(shù)字PCR(dPCR)技術(shù)主要有兩種:微滴式dPCR(ddPCR)和芯片式dPCR(cdPCR)。兩者基本原理相同,由于芯片式dPCR制造芯片的成本較高,目前微滴式dPCR以更低成本、更實用的優(yōu)勢,正越來越受到企業(yè)的認(rèn)可。微滴式dPCR(ddPCR)也在此次疫情防控中有力推動了對疑似疫情感染患者的甄別工作。

主要組成:熒光通道、激光器、光學(xué)檢測器、數(shù)據(jù)采集系統(tǒng)等。
激光器選擇:高功率穩(wěn)定性,光斑高斯分布。
常用波長:405nm,473nm,532nm,639nm等。
2、流式細(xì)胞術(shù)
流式細(xì)胞術(shù)是一項集激光技術(shù)、電子物理、流體力學(xué)、光電測量技術(shù)、計算機技術(shù)、單克隆抗體技術(shù)為一體的新型高科技技術(shù),被譽為實驗室的“CT”,是一種可以對細(xì)胞(或亞細(xì)胞)結(jié)構(gòu)進行快速測量的新型分析技術(shù)和分選技術(shù)。
通過快速測定庫爾特電阻、熒光、光散射和光吸收來定量測定細(xì)胞 DNA含量、細(xì)胞體積、蛋白質(zhì)含量、酶活性、細(xì)胞膜受體和表面抗原等許多重要參數(shù)。根據(jù)這些參數(shù)將不同性質(zhì)的細(xì)胞分開,以獲得供生物學(xué)和醫(yī)學(xué)研究用的純細(xì)胞群體。隨著流式細(xì)胞技術(shù)水平的不斷提高,其應(yīng)用范圍也日益廣泛。流式細(xì)胞術(shù)已普遍應(yīng)用于免疫學(xué)、血液學(xué)、腫瘤學(xué)、細(xì)胞生物學(xué)、細(xì)胞遺傳學(xué)、生物化學(xué)等臨床醫(yī)學(xué)和基礎(chǔ)醫(yī)學(xué)研究領(lǐng)域。

主要組成:液流系統(tǒng),光路系統(tǒng),信號測量和細(xì)胞分選等。
激光器要求:高穩(wěn)定性,低噪聲,定制光斑。
常用波長:355nm,360nm,405nm,473nm,488nm,532nm,561nm,593.5nm,640nm,671nm,785nm等。
3、熒光顯微成像&共聚焦顯微成像
熒光顯微技術(shù)是利用激光作為激發(fā)光源激發(fā)熒光基團產(chǎn)生熒光而成像,產(chǎn)生的熒光波長一般與激發(fā)光不同。它與一般光學(xué)顯微鏡一樣是場激發(fā),因而只能面成像。
共聚焦顯微技術(shù)是在熒光顯微分析技術(shù)的基礎(chǔ)上發(fā)展起來的,利用熒光顯微鏡可以對生物樣品發(fā)出的熒光進行觀察和分析。但是熒光顯微鏡收集到的是樣品的整體熒光,來自樣品內(nèi)不同部位的熒光信號相互干擾、難以區(qū)分,無法獲得準(zhǔn)確的定位和定量信息。
共聚焦顯微技術(shù)的出現(xiàn)很好地解決了這一問題,這一技術(shù)可以獲取細(xì)胞內(nèi)某個薄層面上的熒光信息,而該層以外的信號被消除掉,成像清晰程度大大提高。結(jié)合計算機自動控制,可以對熒光信號的分布、強度和動態(tài)變化進行全方位的分析,得到豐富的信息。與傳統(tǒng)顯微鏡相比,共聚焦顯微鏡可抑制圖像的模糊,獲得清晰的圖像;具有更高的軸向分辨率,并可獲取連續(xù)光學(xué)切片,增加側(cè)向分辨率;點對點掃描,去除了雜散光的影響。其應(yīng)用領(lǐng)域擴展到細(xì)胞學(xué)、微生物學(xué)、發(fā)育生物學(xué)、遺傳學(xué)、神經(jīng)生物學(xué)、生理和病理學(xué)等學(xué)科的研究工作中,成為現(xiàn)代生物學(xué)微觀研究的重要工具。
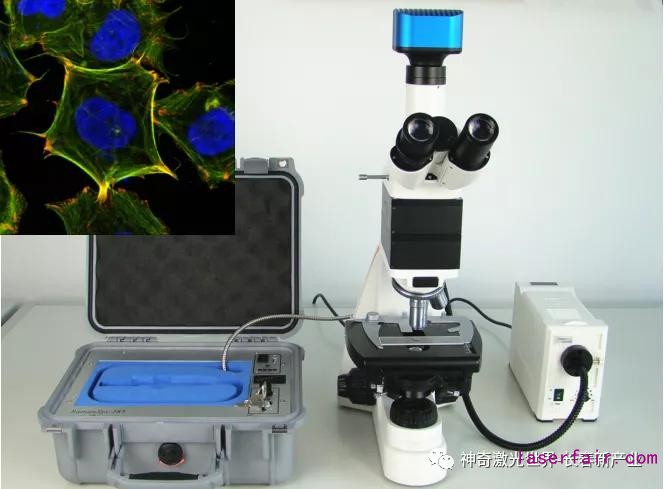
激光器要求:低噪聲,高功率穩(wěn)定性,窄線寬,自由空間/光纖耦合輸出,單波長/多波長可選。
常用波長:266nm,355nm,405nm,473nm,520nm,532nm,561nm,640nm,808nm,980nm等。
4、光聲成像
光聲成像技術(shù)是指:當(dāng)用短脈沖激光輻照生物組織時,位于組織體內(nèi)的吸收體(如腫瘤)吸收脈沖光能量,從而升溫膨脹,產(chǎn)生超聲波;這時,位于組織體表面的超聲探測器可以接收到這些外傳的超聲波,并依據(jù)探測到的光聲信號來重建組織內(nèi)光能吸收分布的圖像。近年來,光聲斷層成像、光聲顯微成像、光聲內(nèi)窺成像發(fā)展迅速,使得532nm高重頻固體脈沖激光器,以及可調(diào)諧激光器得到廣泛應(yīng)用。
對比其他醫(yī)學(xué)成像技術(shù),光聲成像技術(shù)的優(yōu)點及先進性:
(1)使用非電離輻射,是一種無損的醫(yī)學(xué)成像技術(shù)。
(2)結(jié)合了光學(xué)成像的高對比度和超聲成像的高分辨率。解決了光學(xué)成像/超聲成像對比度不高,無法有效監(jiān)測早期腫瘤的問題。
(3)適用于通過內(nèi)源性對比進行功能,代謝和組織學(xué)成像,以及通過外部對比進行分子和細(xì)胞成像。并可與其他成像模式互補并兼容,尤其是光學(xué)成像和超聲成像。
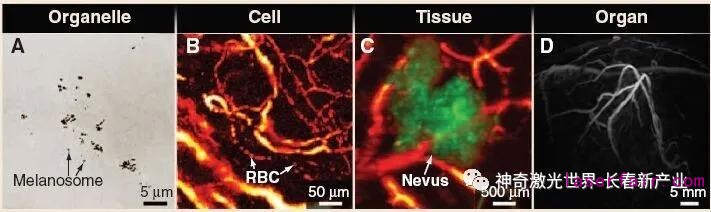
激光器要求:光點穩(wěn)定性好,光斑優(yōu)。
常用波長:266nm,457nm,532nm,660nm,770-840nm可調(diào)諧激光器等。
5、光學(xué)相干層析成像(OCT)
光學(xué)相干層析成像(OCT)是20世紀(jì)90年代逐步發(fā)展而成的一種新的三維層析成像技術(shù)。
OCT基于低相干干涉原理獲得深度方向的層析能力,通過掃描可以重構(gòu)出生物組織或材料內(nèi)部結(jié)構(gòu)的二維或三維圖像。其信號對比度源于生物組織或材料內(nèi)部光學(xué)反射(散射)特性的空間變化。該成像模式的核心部件包括低相干寬帶激光光源、光纖邁克爾遜干涉儀和光電探測器,其軸向分辨率取決于寬帶光源的相干長度,一般可以達(dá)到1-15μm,而徑向分辨率與普通光學(xué)顯微鏡類似,決定于樣品內(nèi)部聚焦光斑的尺寸,一般也在微米量級。
OCT具有非接觸、非侵入、成像速度快(實時動態(tài)成像)、探測靈敏度高等優(yōu)點。目前,OCT技術(shù)已經(jīng)在臨床診療與科學(xué)研究中獲得了廣泛的應(yīng)用,如眼科醫(yī)療,視網(wǎng)膜病、牙科齲齒的檢測、心血管疾病探查、胃腸道疾病檢測、乳腺癌早期診斷等,具有其他檢測設(shè)備無法比擬的高分辨率和精準(zhǔn)度。
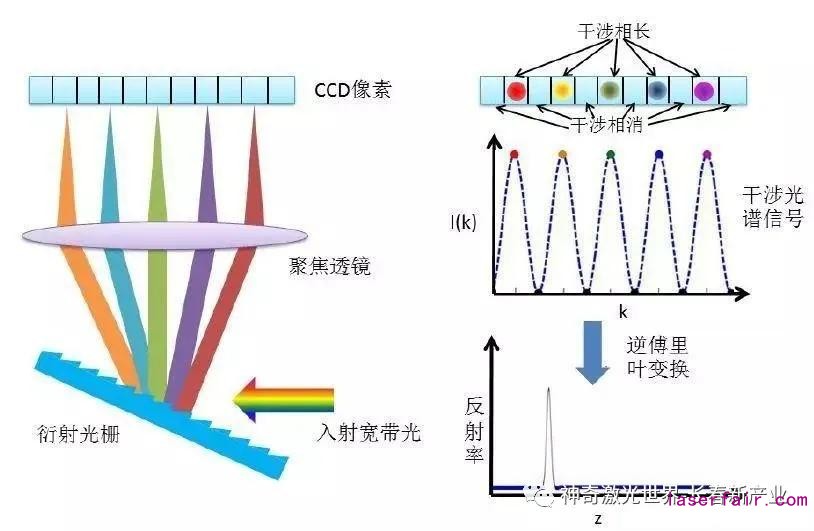
主要組成:低相干寬帶激光光源,光纖邁克爾遜干涉儀,光電探測器等。
激光器要求:較寬的頻譜寬度,高輸出功率,高功率穩(wěn)定性,易于耦合。
常用波長:1470nm,1550nm,1710nm等。
6、DNA測序
DNA測序是指通過分析特定DNA片段堿基序列,也就是腺嘌呤(A)、胸腺嘧啶(T)、胞嘧啶(C)與鳥嘌呤的(G)排列方式,獲得生物遺傳信息的方法。
DNA測序采用鏈終止法,在DNA轉(zhuǎn)錄末端引入帶有熒光標(biāo)記的寡核苷酸,此時DNA被分成了長度不同的單鏈;再使其通過激光聚焦光束,不同熒光素會發(fā)出不同顏色熒光,達(dá)到標(biāo)記核苷酸排序的目的。DNA測序的出現(xiàn)極大地推動了生物學(xué)和醫(yī)學(xué)的研究和發(fā)現(xiàn)。

激光器要求:高波長穩(wěn)定性,高功率,優(yōu)光斑均勻性。
常用波長:473nm,488nm,505nm,514.5nm,532nm,561nm,577nm,639.5nm等。
7、光鑷
光鑷(Optical tweezers)技術(shù)基于光輻射壓力與單光束梯度力光阱,是用物鏡下高度匯聚的激光形成的三維梯度勢阱來俘獲、操縱和測量微小顆粒力學(xué)特性的光學(xué)技術(shù)。光鑷的應(yīng)用可歸納為四類,即光鑷與細(xì)胞生物學(xué)、光鑷與單分子生物學(xué)、光鑷與膠體科學(xué)以及光鑷與物理學(xué)4個學(xué)科領(lǐng)域。光鑷技術(shù)在這些領(lǐng)域已成功解決了許多的重大科學(xué)問題。經(jīng)過近30年的發(fā)展,光鑷技術(shù)得到了極快的發(fā)展。由過去簡單的單光鑷演化出了許多其他的類型,極大地擴大了光鑷技術(shù)在現(xiàn)代科學(xué)技術(shù)領(lǐng)域的應(yīng)用。
1)全息光鑷:可以自由控制多個粒子,使得粒子的融合、吸附以及粒子間或粒子與表面的相互作用研究得到簡化。利用全息元件或空間光調(diào)制器(SLM)所形成的全息光鑷,在多粒子操控方面的優(yōu)勢,為光鑷技術(shù)走向?qū)嵱没⒁?guī)模工業(yè)生產(chǎn)打開了新局面,是目前光鑷家族極具活力的成員。
2)等離子體光鑷:用最小激光能量鑷取最小微粒的納米光鑷。通過采用等離子體光鑷結(jié)構(gòu),被捕獲的納米顆粒的運動被限制在等離子體區(qū)域,該區(qū)域比激光的衍射限制區(qū)域小得多,使得捕獲更加穩(wěn)定。等離子體光鑷技術(shù)可以克服自由空間衍射帶來的限制,增強阱內(nèi)的局部光強度,能解決目前光鑷技術(shù)研究中存在的進場光鑷倏逝場偏弱、金屬顆粒難以捕獲等問題。等離子光鑷技術(shù)不僅將加速生命/納米/材料科學(xué)的研究進展,而且還將產(chǎn)生新的功能材料、納米醫(yī)學(xué)和診斷工具。這一科學(xué)領(lǐng)域在未來將繼續(xù)迅速發(fā)展。
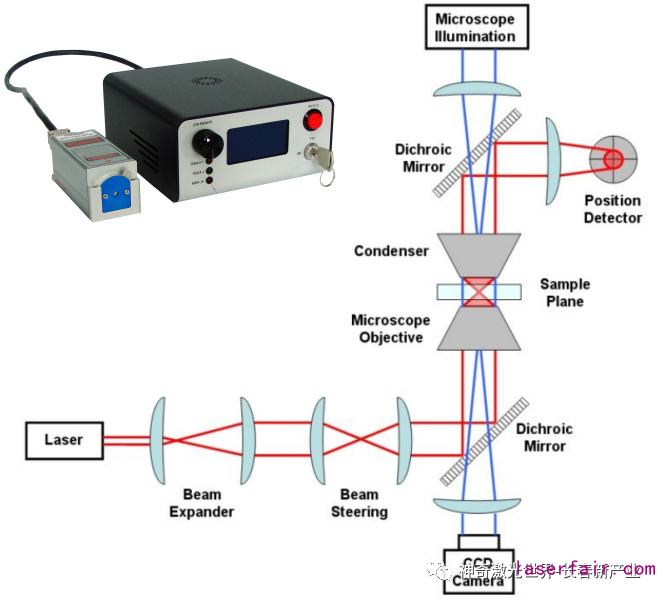
激光器要求:低噪聲,高功率穩(wěn)定性。
常用波長:532nm、635nm、1064nm等。
轉(zhuǎn)載請注明出處。









 相關(guān)文章
相關(guān)文章
 熱門資訊
熱門資訊
 精彩導(dǎo)讀
精彩導(dǎo)讀























 關(guān)注我們
關(guān)注我們




